またひとつ、見逃せない承認情報が出てきました。
レチファンリマブ【ジニイズ点滴静注500mg】が、
「切除不能な進行・再発の肛門管扁平上皮癌」を対象として、製造販売承認を取得しています。

今回のポイントは、
ただ新しい薬が出た、というだけではありません。
肛門管扁平上皮癌という、もともと症例数が多くない領域で、免疫療法が一次治療の前のほうに入ってきたことが、かなり大きな変化なんですよね。日本では肛門がん全体のうち腺がんがおよそ8割、扁平上皮がんがおよそ2割とされていて、欧米よりも扁平上皮癌の割合が低いことも、この領域の情報がやや追いにくい背景にあります。
今回は
- ジニイズの承認内容
- ガイドライン上の位置づけ
- 現場で押さえたいポイント
を、かんたんに整理していきます。
レチファンリマブ【ジニイズ点滴静注】今回の承認内容は?
今回示されている効能又は効果は、
「切除不能な進行・再発の肛門管扁平上皮癌」です。
さらに用法・用量としては、
パクリタキセルおよびカルボプラチンとの併用において、通常、成人にはレチファンリマブとして1回500mgを4週間間隔で30分かけて点滴静注する
と整理されています。
つまり今回の承認は、
- 対象疾患:切除不能な進行・再発の肛門管扁平上皮癌
- 投与薬剤:レチファンリマブ【ジニイズ】
- 使い方:カルボプラチン+パクリタキセル併用
- 投与量:500mg
- 投与間隔:4週間ごと
- 投与時間:30分かけて点滴
という理解で押さえるとわかりやすいです。

肛門管扁平上皮癌って、どんな立ち位置?
肛門がんはかなりまれながんで、国立がん研究センターでも全悪性腫瘍の0.1%、大腸がんの中でも2%程度とされています。日本ではその中でも扁平上皮がんは約2割で、欧米では肛門がんの多くが扁平上皮癌であるのに対して、日本ではやや事情が違います。
ここ、地味に大事です。
なぜかというと、
日本では症例数が少ないぶん、肛門管扁平上皮癌の治療は「国内の大腸癌文脈」だけでなく、海外ガイドラインの流れもかなり重要だからです。大腸癌研究会の資料でも、欧米では肛門管癌の多くが扁平上皮癌であり、一方で本邦では扁平上皮癌は低率であること、そして肛門管扁平上皮癌では放射線化学療法が主体になってきていることが示されています。
ガイドラインでは、まず化学放射線療法が重要
日本の大腸癌治療ガイドライン 2024年版では、肛門管扁平上皮癌に対する化学放射線療法に関する新規CQが追加されています。これは、それだけこの領域を独立して扱う必要性が高まっている、という見方もできます。
実際、同ガイドラインでは、
Ⅰ期の肛門管扁平上皮癌に対しては化学放射線療法を行うことが望ましいと考えられる一方、併用化学療法の遂行可否や腫瘍径、分化度などによっては放射線治療単独や局所切除も選択肢になり得るとされています。ガイドライン中では、Ⅰ期症例のレビューで5年全生存率は化学放射線療法のほうが良好だったことも紹介されています。
なので、まず大前提としては、
肛門管扁平上皮癌では、局所病変に対して化学放射線療法がかなり大きな柱になっている
ここを押さえておくと、今回のレチファンリマブ【ジニイズ】承認の意味が見えやすくなります。
じゃあ「切除不能な進行・再発」ではどう考える?
今回の承認対象は、
**「切除不能な進行・再発」**です。
この段階になると、局所治療だけではなく、全身薬物療法の意味合いが一気に大きくなります。
そして海外では、この領域の治療の流れがかなり整理されてきています。FDAは2025年5月、retifanlimab-dlwr(Zynyz)をカルボプラチン+パクリタキセルとの併用で、切除不能な局所再発または転移性の肛門管扁平上皮癌の一次治療として承認しました。
さらにFDAの審査内容では、試験で用いられたレジメンとして
カルボプラチン AUC 5をDay1、パクリタキセル80mg/m²をDay1・8・15、retifanlimab 500mgを4週ごと
という形が示されています。これは今回の日本向けPDFに載っていたスケジュールと整合する内容です。
レチファンリマブ【ジニイズ】は、どんな薬なの?
レチファンリマブ【ジニイズ】は、
抗悪性腫瘍剤・ヒト化抗ヒトPD-1モノクローナル抗体
とされています。さらに、PD-1とそのリガンド(PD-L1、PD-L2)との結合を阻害することで、T細胞の活性化や腫瘍細胞に対する細胞傷害活性を亢進し、腫瘍増殖を抑制すると説明されています。
ざっくり言えば、
免疫チェックポイント阻害薬のひとつで、
PD-1を標的にして、抗腫瘍免疫を後押しするタイプの薬
という理解でOKです。
海外ガイドラインでは、一次治療の前線に入ってきている
NCCNの患者向けガイドラインでは、転移性肛門がんの preferred first-line regimenとして、
carboplatin + paclitaxel + retifanlimab-dlwr
が掲載されています。
ここ、かなり象徴的です。
少し前までのイメージだと、
まず細胞障害性抗がん薬中心
→ その後に免疫チェックポイント阻害薬
という流れで捉えられることが多かったのですが、retifanlimabは一次治療からカルボプラチン+パクリタキセルに上乗せする形で位置づけられ始めています。FDAの承認内容も、まさにその流れです。
つまり今回の承認は、
免疫療法が「後ろのラインの選択肢」から、「最初から組み込む治療」へ一歩前に出てきた
そう見ると、かなりインパクトがあります。
今や、免疫チェックポイント阻害薬ことICIは、ある程度のがん種で第一治療に位置付けられるようになりました。
レチファンリマブの投与スケジュールを、実務目線でざっくり整理
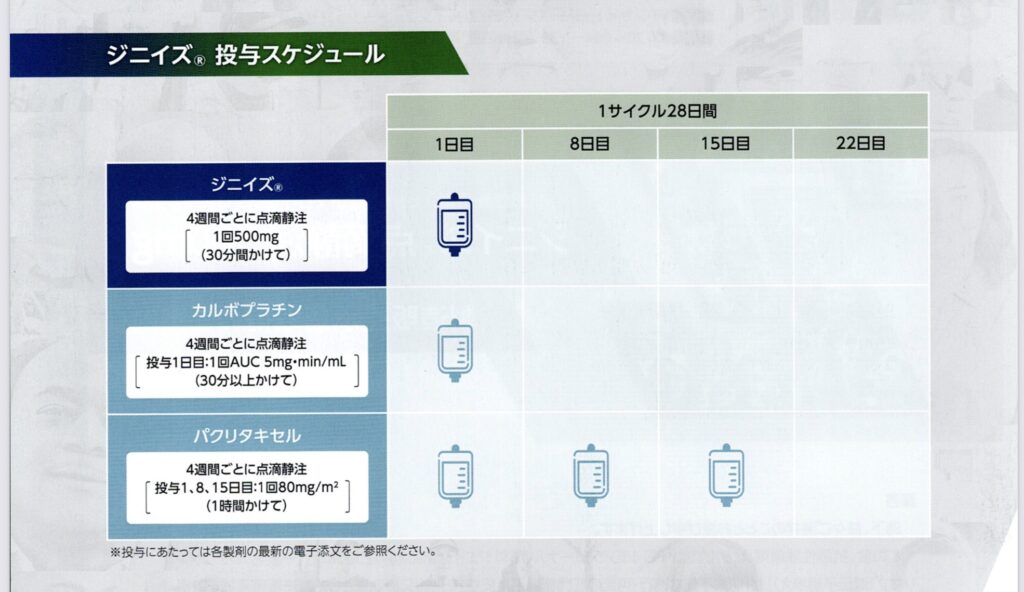
上記スケジュール表では、1サイクル28日として次のように整理されています。
1サイクル28日
- ジニイズ®:Day1
- 1回500mg
- 30分かけて点滴
- 4週ごと
- カルボプラチン:Day1
- 1回AUC 5 mg・min/mL
- 30分以上かけて投与
- パクリタキセル:Day1、8、15
- 1回80mg/m²
- 1時間かけて投与
この形なので、外来のイメージとしては
「Day1に全部入る、でもPTXはDay8・15にも来る」
という認識がしっくりきます。
薬剤師的に押さえるレチファンリマブのポイント
1.「単剤で覚えない」が大事
今回の承認内容は、カルボプラチン+パクリタキセル併用が前提です。
なので、ジニイズだけ単独で切り出して覚えるより、レジメン全体で理解するほうが実務では役立ちます。
2.疾患名はかなり限定的
対象はあくまで
切除不能な進行・再発の肛門管扁平上皮癌。
「肛門がん全般」ではなく、
扁平上皮癌であること、
切除不能であること、
進行・再発であること、
この3点セットで読むのが大事です。日本では肛門がん全体では腺がんの割合が高いので、なおさらこの整理は重要です。
3.局所治療の世界観との違いを意識する
肛門管扁平上皮癌は、局所病変では化学放射線療法が大きな柱です。だからこそ、今回の承認は局所治療の話ではなく、切除不能な進行・再発例における全身薬物療法のアップデートとして理解するのが自然です。
4.“免疫療法が前に来た”という見方がわかりやすい
NCCNでもretifanlimab併用が一次治療のpreferred regimenとして示され、FDAでも一次治療として承認されています。なので今回の承認は、免疫療法の位置づけが前進したという印象になります。

レチファンリマブ【ジニイズ】のまとめ
今回のジニイズ®点滴静注500mgの承認をひとことで言うと、
切除不能な進行・再発の肛門管扁平上皮癌に対して、
カルボプラチン+パクリタキセルに免疫療法を組み合わせる流れが、
よりはっきり見えるようになった承認
という感じです。
日本のガイドラインでは、肛門管扁平上皮癌に対して化学放射線療法の重要性が明確に意識されていて、2024年版ではこの領域に関する新規CQも追加されています。
そのうえで、切除不能な進行・再発例では、海外の承認やガイドラインを踏まえた全身薬物療法のアップデートが重要になってきます。
今回の内容を実務的に覚えるなら、
- 適応:切除不能な進行・再発の肛門管扁平上皮癌
- 併用:カルボプラチン+パクリタキセル
- ジニイズ:500mg、4週間ごと、30分点滴
- 位置づけ:免疫療法が一次治療から組み込まれる流れ
この4点でかなり整理しやすいと思います。



コメント